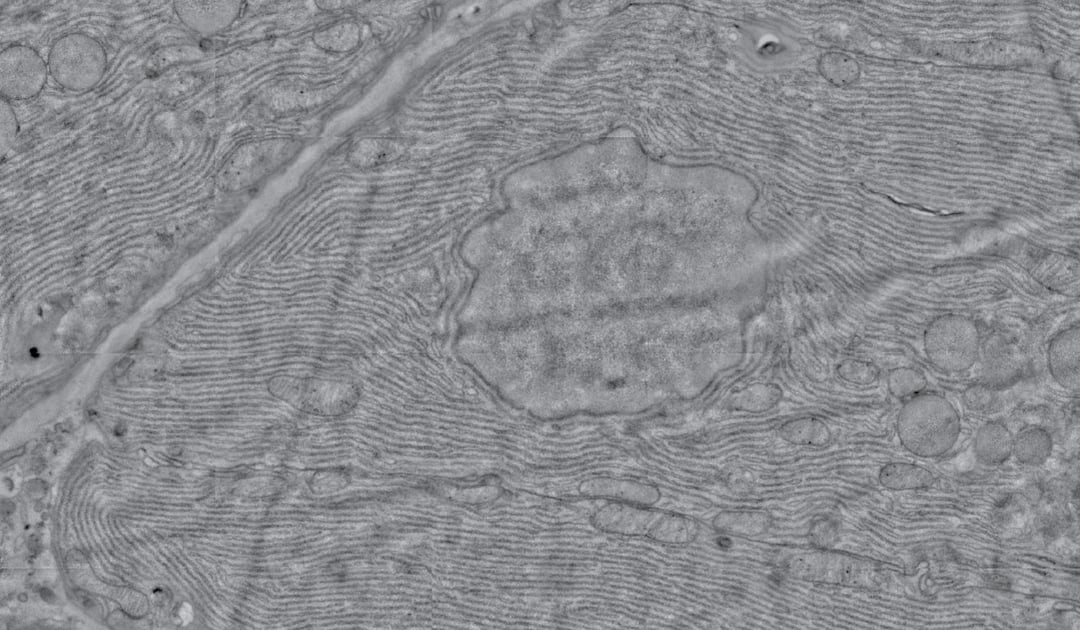
近几十年来,电子显微镜已被证明是解析纳米级结构的好工具。电子显微镜正逐步被用于大规模的生物项目:三维结构成像和大面积映射。这两种项目都希望做到大面积覆盖或跨越三维空间,在解析纳米级细节的同时,又能将观察结果置于更大的样本环境中。正是由于自动化的增加和图像处理工作的完善,这些大规模的成像项目现如今才会成为可行之选,而这些项目提供的信息已经被证明对多种研究领域非常有益,包括发育和细胞生物学、神经科学和病理学[1,2,3]。
大规模成像需要在比显微镜视场大几个数量级的面积或体积上实现纳米级分辨率,这无疑对常规扫描电镜形成了巨大的挑战。
最大的挑战之一是当前扫描电镜系统的速度有限。由于它们的采集速率有限,显微镜操作人员被迫在成像区域的尺寸和符合可视化细节要求的分辨率之间取得平衡。尽管尽了最大的努力,但是当需要高分辨率数据时,大型项目仍需要数天甚至数月才能在多台机器上进行连续成像[4,5,6]。这会给成像设备带来后勤问题,因为成像设备只能为少数几个用户处理这些项目。
大规模成像的另一个挑战是成像周期中的时间耗费,这会影响显微镜的持续高通量。通量通常被宣传为显微镜的峰值采集速率(通常表示为每秒像素数)。但是,由于样本转换、载物台移动和图像质量调整导致的成像周期耗费,在成像项目期间很少会达到该峰值采集速率。成像周期中的这些步骤至少占显微镜时间的30-40% [3,7,8]。因此,一种能最小化显微镜这些时间耗费的高效采集程序对于最大化电镜工作流程的持续处理量至关重要。
最后,传统的显微镜还没有实现足够大的自动化而无法自动运行。对于大规模应用来说,区域选择是必需的,这通常由操作员根据问题或项目手动完成。另外,如果没有操作员来照料系统进行诸如样本交换、成像区域选择、光束聚焦和对准等步骤,常规显微镜通常不会长时间运行,从而限制了其扩展成像运行的潜力。在某些糟糕的情形下,这甚至意味着显微镜只能在操作员的工作时间内产生数据,而极大地影响其生产量。
对于提高电子显微镜的处理量、可靠性和自动化的需求表明了研究领域中正需要一种新颖的大规模成像方法,近期Delmic提出了自动超快体扫描电镜的解决方案用以应对大规模电子成像的速度限制。目前,Delmic正在与Thermo Fisher、TU Delft和Technolution合作开发高度自动化和可靠的工作流程。凭借其极强的易用性,自动超快体扫描电镜可以服务于非常广泛的用户。
在接下来的几个月中,我们将重点介绍超快体扫描电镜成像的其他信息以及我们目前正在研究的项目。想在第一时间了解我们最新开发的系统吗?请以下的点击的按钮:
References:
[1] Peddie, C. J., & Collinson, L. M. (2014). Exploring the third dimension: volume electron microscopy comes of age. Micron (Oxford, England : 1993), 61, 9–19. https://doi.org/10.1016/j.micron.2014.01.009
[2] Sokol, E., Kramer, D., Diercks, G. F. H., Kuipers, J., Jonkman, M. F., Pas, H. H., & Giepmans, B. N. G. (2015). Large-scale electron microscopy maps of patient skin and mucosa provide insight into pathogenesis of blistering diseases. Journal of Investigative Dermatology, 135(7), 1763–1770. https://doi.org/10.1038/jid.2015.109
[3] Titze, B., & Genoud, C. (2016). Volume scanning electron microscopy for imaging biological ultrastructure. Biology of the Cell, 108(11), 307–323. https://doi.org/10.1111/boc.201600024
[4] Hildebrand, D. G. C., Cicconet, M., Torres, R. M., Choi, W., Quan, T. M., Moon, J., Wetzel, A. W., Scott Champion, A., Graham, B. J., Randlett, O., Plummer, G. S., Portugues, R., Bianco, I. H., Saalfeld, S., Baden, A. D., Lillaney, K., Burns, R., Vogelstein, J. T., Schier, A. F., … Engert, F. (2017). Whole-brain serial-section electron microscopy in larval zebrafish. Nature, 545(7654), 345–349. https://doi.org/10.1038/nature22356
[5] Xu, C. S., Hayworth, K. J., Lu, Z., Grob, P., Hassan, A. M., García-Cerdán, J. G., Niyogi, K. K., Nogales, E., Weinberg, R. J., & Hess, H. F. (2017). Enhanced FIB-SEM systems for large-volume 3D imaging. ELife, 6, 1–36. https://doi.org/10.7554/eLife.25916
[6] Yin, W., Brittain, D., Borseth, J., Scott, M. E., Williams, D., Perkins, J., Own, C., Murfitt, M., Torres, R. M., Kapner, D., Bleckert, A., Castelli, D., Reid, D., Lee, W.-C. A., Graham, B. J., Takeno, M., Bumbarger, D. J., Farrell, C., Reid, R. C., & Costa, N. M. da. (2019). A Petascale Automated Imaging Pipeline for Mapping Neuronal Circuits with High-throughput Transmission Electron Microscopy. BioRxiv, 791889. https://doi.org/10.1101/791889
[7] Briggman, K. L., & Bock, D. D. (2012). Volume electron microscopy for neuronal circuit reconstruction. Current Opinion in Neurobiology, 22(1), 154–161. https://doi.org/10.1016/j.conb.2011.10.022
[8] Zheng, Z., Lauritzen, J. S., Perlman, E., Robinson, C. G., Nichols, M., Milkie, D., Torrens, O., Price, J., Fisher, C. B., Sharifi, N., Calle-Schuler, S. A., Kmecova, L., Ali, I. J., Karsh, B., Trautman, E. T., Bogovic, J. A., Hanslovsky, P., Jefferis, G. S. X. E., Kazhdan, M., … Bock, D. D. (2018). A Complete Electron Microscopy Volume of the Brain of Adult Drosophila melanogaster. Cell, 174(3), 730-743.e22. https://doi.org/10.1016/j.cell.2018.06.019
.png)